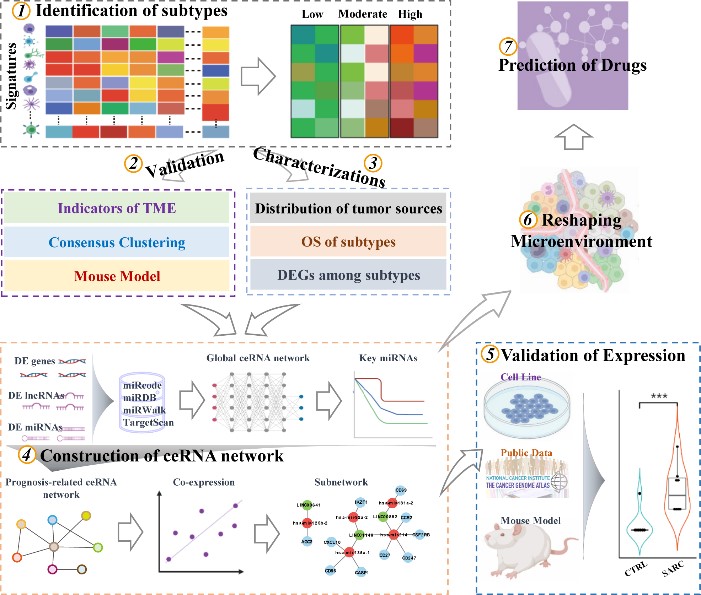
澳門大學健康科學學院副教授趙琦、院長鄧初夏聯同該院時任學院教授張曉華的團隊從腫瘤免疫微環境的角度定義了肉瘤的亞型,並識別出腫瘤免疫微環境的調控ceRNA網絡,通過分析疾病的分子機理及關鍵因子的數據,最終提出了潛在的治療藥物,為肉瘤的臨床治療提供了新的思路。研究成果已發表於國際知名學術期刊《臨床癌症研究》。
競爭性內源RNA(ceRNA)是近幾年來備受學術關注的對象。由此產生的ceRNA網絡假設詮釋了一種比miRNA調控網絡更為精細複雜的基因表達調控模式,涉及更多的RNA分子,包括mRNA、編碼基因假基因、長鏈非編碼和miRNA等。ceRNA網絡調控的關鍵在於通過競爭性結合miRNA進而調控其靶基因的表達。這種調控模式的揭示有助於從更深層面上挖掘基因功能和調控機制,以便於更深入全面的解析細胞發育、疾病分子機理等很多重要的生物學現象。同時,ceRNA網絡分析得到的關鍵因子也是潛在的預後標記物和治療靶點。目前,在肝癌、乳腺癌、肺癌等多種腫瘤中證實了ceRNA調控機制在腫瘤發生、發展及轉移中的作用。
另外,腫瘤微環境(tumor microenvironment, TME)是一種由腫瘤細胞誘導,在其周圍產生大量的生長因子、趨化因子以及基質降解酶的綜合體系,當中存在豐富的腫瘤細胞、基質細胞、細胞因子和免疫細胞等成分。這些成分與腫瘤細胞密切相互作用,影響腫瘤的生長、進展和轉移。近年來,研究發現ceRNA網絡調控與腫瘤微環境關係密切,例如ceRNA網絡可顯著區分骨肉瘤和間充質幹細胞,以及在結直腸癌中發現與免疫浸潤相關的預後ceRNA網絡等。然而,在軟組織肉瘤中,ceRNA網絡與腫瘤微環境的調控和重構關係還沒有明確的研究,關於ceRNA網絡對肉瘤發展的影響和ceRNA網絡在肉瘤病人中的預後價值缺乏充分的研究。
基於以上論述,研究團隊觀察到在軟組織肉瘤中普遍存在腫瘤免疫浸潤低、中、高三種亞型,且不同亞型病人之間的總體生存率差異顯著。團隊通過結合病人的生存數據,在亞型間識別了關鍵的ceRNA網絡,發現該關鍵ceRNA網絡具有潛在的預後價值,並進一步發現該關鍵ceRNA網絡的調控與腫瘤微環境的形成和重構密切相關。團隊同時結合免疫分型特徵,利用藥物/小分子功能注釋及其與基因互作關係數據庫,找到一種潛在的治療藥物——組蛋白脫乙酰酶抑制劑Trichostatin A。經動物模型和體外實驗驗證,該藥物能有效降低體內組蛋白脫乙酰酶活性,抑制腫瘤生長。而該研究中識別到的關鍵ceRNA網絡中的因子,極有可能就是Trichostatin A在肉瘤中的作用靶點。研究為肉瘤病人的診療提供了新的理論依據和思路。
是次研究的通訊作者為鄧初夏、趙琦和張曉華,澳大健康科學學院博士畢業生冷棟樑、博士生楊子怡和研究助理教授孫恆為共同第一作者,澳大健康科學學院教授陳國凱、博士後宋程程和研究助理葉家宇也對研究做出了重要的貢獻。研究得到國家重點研發計劃(檔案編號:2019YFA0904400)、澳門特別行政區科技發展基金(檔案編號:FDCT/0043/2021/A1、FDCT/0004/2019/AFJ和0065/2021/A)、廣東省自然科學基金(檔案編號:2023A1515010549)、深圳市科技項目(檔案編號:SGDX2020110309280301)、澳門大學(檔案編號:MYRG2022-00143-FHS)、何鴻燊博士醫療拓展基因會(檔案編號:SHMDF-VSEP/2022/002)、美國國立衛生研究院(檔案編號:UL1TR001998、1U01DK135111和OT2HL161847)、華盛頓大學DRC(檔案編號:P30 DK020579)等項目的聯合資助。全文可瀏覽:https://doi.org/10.1158/1078-0432.CCR-22-3396。
| 新聞來源:健康科學學院 | |
| 媒體聯繫: | |
| 澳門大學傳訊部 | |
| 李巧雲 | 電話:(853) 88228004 |
| 梁雄業 | 電話:(853) 88228322 |
| 電郵: | prs.media@um.edu.mo |